لأول مرة استخدام تقنية كريسبر (CRISPR) لتعديل جنين بشري في الولايات المتحدة
9 أغسطس، 2017
الطب
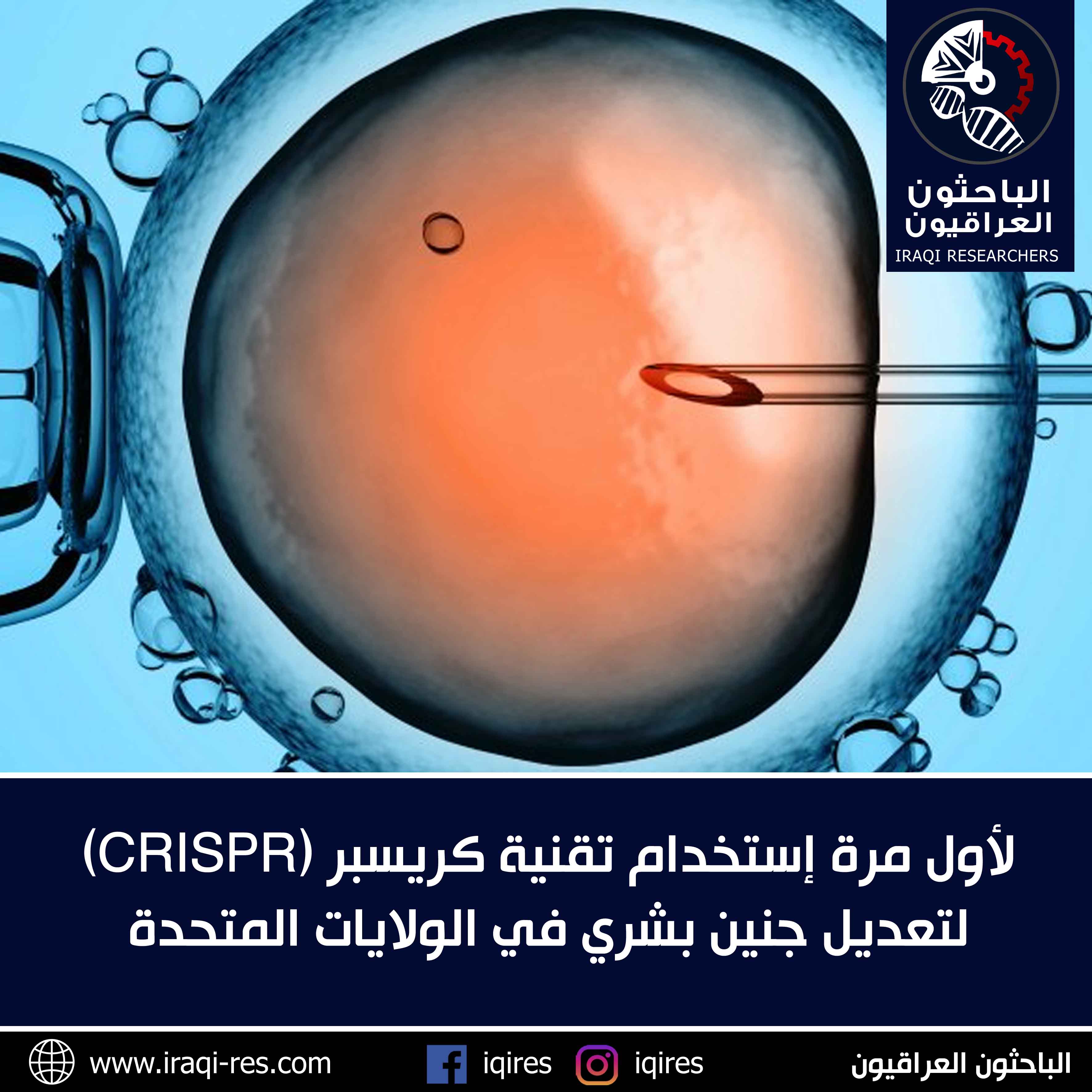
قام الباحثون في بورتلاند بولاية أوريغون، ولأول مرة، بتعديل جنينٍ بشري في الولايات المتحدة.
يضاف هذا العمل إلى ما تعدنا به تقنية كريسبر، وهو يمثل خطوةً مهمةً نحو ولادة أول البشر المعدلين وراثيًا.
معظمنا يعرف الآن ما هي تقنية كريسبر لتعديل الجينات. على الأقل سمعنا عن هذه التكنولوجيا الثورية التي تسمح لنا بتعديل الحمض النووي DNA — شيفرة الحياة ذاتها.
يومًا ما، ستمكننا كريسبر من حذف الجينات للقضاء على الأمراض الوراثية، وإضافة جينات جديدة لتحسين مختلف الوظائف الحيوية على نحوٍ واسعٍ، أو حتى تعديل الأجنة البشرية وراثيًا من أجل خلق نوعٍ جديدٍ تمامًا من البشر…من البشر الخارقين.
لكن أولاً، لدينا الكثير من البحوث للقيام بها.
وهذا يقودنا إلى يومنا هذا. أكدت التقارير من معهد ماساتشوستس للتكنولوجيا (MIT) أن أول محاولة لخلق أجنة بشرية معدلة وراثيًا في الولايات المتحدة قد تم تنفيذها من قبل فريق من الباحثين في بورتلاند، أوريغون.
وقال جون وو (Jun Wu)، الذي لعب دورًا في المشروع، وهو معاون في معهد سولك: “حسب حد علمي، أن هذه ستكون أول دراسة يتم الإعلان عنها في الولايات المتحدة.”
لقد قاد العمل شوكرات ميتاليبوف (Shoukhrat Mitalipov)، من جامعة أوريغون للصحة والعلوم.
رغم قلة التفاصيل في هذه المرحلة، تؤكد مصادر مُطَلعة على العمل أن البحث يتضمن تعديل الحمض النووي لأجنة مكونة من خلية واحدة فقط باستخدام تقنية كريسبر.
كما يعتقد أن ميتاليبوف قد حطم رقمًا قياسيًا بطريقتين بارزتين:
• حطم رقمًا قياسيًا بعدد الأجنة في التجربة.
• وهو أول باحث يثبت بشكل قاطع إمكانية تصحيح الجينات المعيبة التي تسبب الأمراض الوراثية بأمانٍ وكفاءةٍ.
وذلك أمر جدير بالملاحظة لأن على الرغم من وجودها منذ عدة سنوات، لا تزال تقنية كريسبر أداة جديدة إلى أبعد حد — أداة يمكن أن تؤدي إلى نتائج غير مقصودة.
وكما كشف عمل سابق نُشِر في مجلة (Nature Methods)، يمكن أن تؤدي هذه التقنية إلى طفرات غير مقصودة في الجينات.
غير أن الباحثين استعرضوا العمل لاحقًا في مؤسسةٍ أخرى وأثارت النتائج تساؤلهم.
وتبقى أن نرى ما إذا كان سيتم تصحيح الدراسة الأصلية أو التراجع عنها، ولكن هذا التقدم يسلط الضوء على أهمية النقد الذي يقدمه الزملاء في العلم.
وبهذا الصدد، يسهل لنا عمل ميتاليبوف فهم كيفية عمل كريسبر في البشر على نحوٍ دقيقٍ، ويكشف أن من الممكن تجنُب كلٌ من الفسيفساء الجينية (Genetic mosaicism: ونعني بها التغيرات التي تحدث في بعض خلايا الجنين وليس جميعها) والتأثير خارج الهدف (Off-target effect: التأثير على جينات أخرى غير الجين المستهدف).
من المهم ملاحظة أنه لم يسمح لأي من الأجنة بالاستمرار بالنمو لأكثر من بضعة أيام، ولم تكن للفريق النية في زرعها داخل الرحم.
ومع ذلك، يبدو أن هذا يرجع في الغالب إلى قضايا تنظيمية جارية، وليس إلى مسائل تتعلق بالتكنولوجيا نفسها.
في الولايات المتحدة، تم منع جميع الجهود المبذولة لتحويل الأجنة المعدلة إلى أطفال — السماح بمدة الحمل الكاملة — من قبل الكونغرس، والذي أضاف القول إلى وزارة الصحة والخدمات البشرية لتمويل مشروع قانون يمنع الموافقة على أي من هذه التجارب السريرية.
ومع ذلك، فإن إمكانيات نظام كريسبر كتكنولوجيا لتعديل الجينات أمر لا يمكن إنكاره. كما ذكر سابقا، فقد شهدت نجاحًا في تطوير العلاجات المحتملة للسرطان، وفي جعل الحيوانات مقاومة للأمراض، كما أنها تَعِد بإستبدال المضادات الحيوية كليًا.
يضاف هذا العمل إلى ما تعدنا به تقنية كريسبر، وهو يمثل خطوةً مهمةً نحو ولادة أول البشر المعدلين وراثيًا.
ترجمة: Banen Adel
تدقيق علمي: Muhammad Basim
تدقيق لغوي: Tabarek A. Abdulabbas
تصميم: Tabarek A. Abdulabbas
المصدر: هنا
 الباحثون العراقيون Iraqi Researchers
الباحثون العراقيون Iraqi Researchers


